一个诺奖反应串起多个苯环 |
您所在的位置:网站首页 › joseph conrad简介 › 一个诺奖反应串起多个苯环 |
一个诺奖反应串起多个苯环
|
一个诺奖反应串起多个苯环
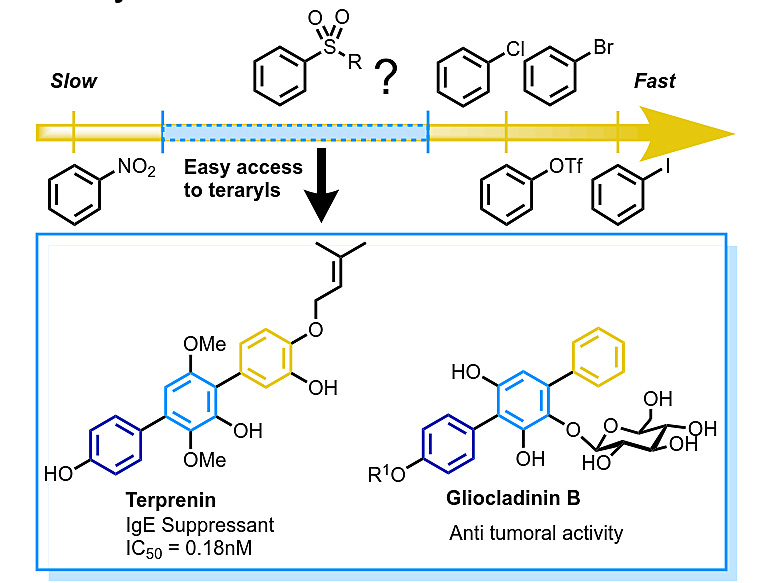
Suzuki-Miyaura偶联反应(SMC)在学术界和工业界被广泛用于生物活性分子、农用化学品和有机材料的合成,并于2010年获得了诺贝尔化学奖。在联芳基化合物合成中,目前SMC最常用的亲电偶联配偶体(coupling partners)是芳基卤代物(-I、-Br、-Cl)或拟卤代物(-OTf)。该反应已经发展的非常完善,但由于不同亲电试剂之间活性差异小且不可预测,目前还很难使用简洁、迭代的SMC反应序列来获得非对称的三联和四联芳基化合物。卤代物和拟卤代物已成功地用于连续交叉偶联反应,如Schoenebeck等人报道的连续Negishi偶联反应。然而,除了少数例子之外,连续SMC反应合成聚芳烃仍主要局限于特定底物或需要迭代的官能团转化。三联苯化合物由于具有药用潜力而备受化学家们的关注,在三联苯的合成方面,芳基砜的SMC反应很有可能大有用武之地(图1a)。芳基砜提供的合成调节砌块可以调节底物的反应性,并且可以导向邻位、间位和对位官能团化,同时在水解条件下保持稳定。然而,目前还没有芳基砜SMC反应的通用方法。 最近,法国斯特拉斯堡大学Joseph Moran教授课题组报道了(杂)芳基砜的SMC反应的发现和发展,该反应活性介于(拟)卤代芳烃和硝基芳烃之间,从而可以通过快速连续偶联反应实现非对称三联和四联芳基化合物的迭代合成。相关论文发表于Angew. Chem. Int. Ed.。
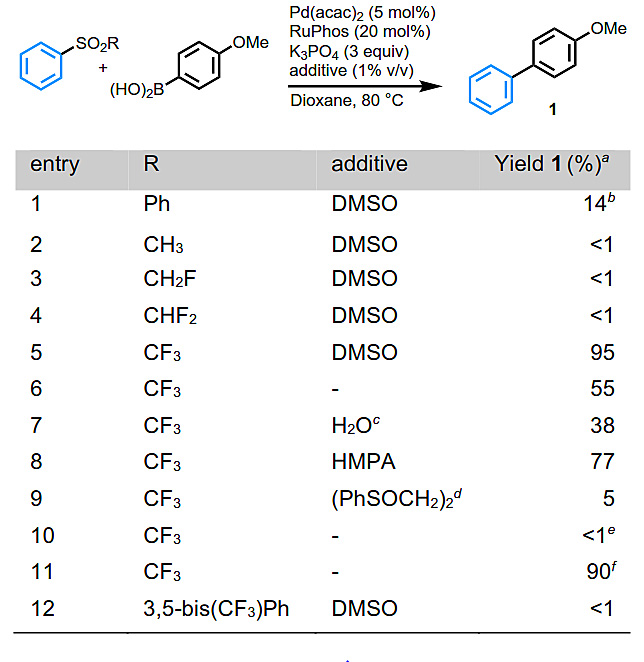
图1. Suzuki-Miyaura反应中亲电试剂的相对反应活性。图片来源:Angew. Chem. Int. Ed. 作者的初步实验侧重于确定能够用作亲电偶联配偶体的芳基砜(图2)。RuPhos作配体,在K3PO4、催化量Pd(acac)2和少量DMSO存在下时,二苯砜与4-甲氧基苯硼酸在130 °C(entry 1)发生偶联。苯基甲基砜及其单氟和二氟化类似物不反应,但苯基三氟甲基砜即使在80 °C时也能顺利发生偶联。DMSO作为添加剂可能是高收率的重要因素,能够增溶无机碱的其他添加剂也有类似的作用,但效果较小,而水则不利于反应。在这些条件下,三氟甲基亚砜或三氟甲基酮,没有发生偶联反应。
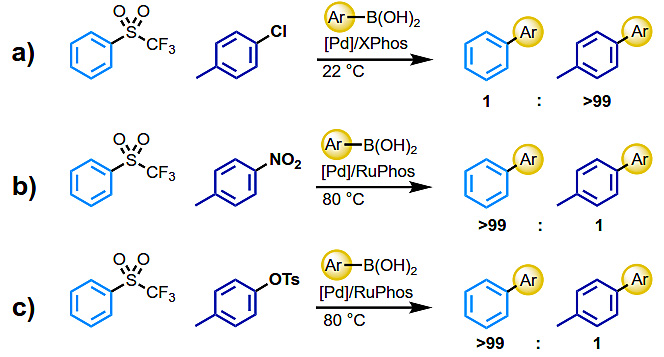
图2. 反应条件优化。图片来源:Angew. Chem. Int. Ed. 将芳基砜与其他亲电试剂进行比较的竞争实验表明,在标准条件下,芳基砜SMC 的反应活性至少比芳基氯代物慢两个数量级,但至少比硝基芳烃和芳基对甲苯磺酸酯快两个数量级。使用 Xphos 作为配体代替 RuPhos,在 80 °C下并不能实现砜的交叉偶联。
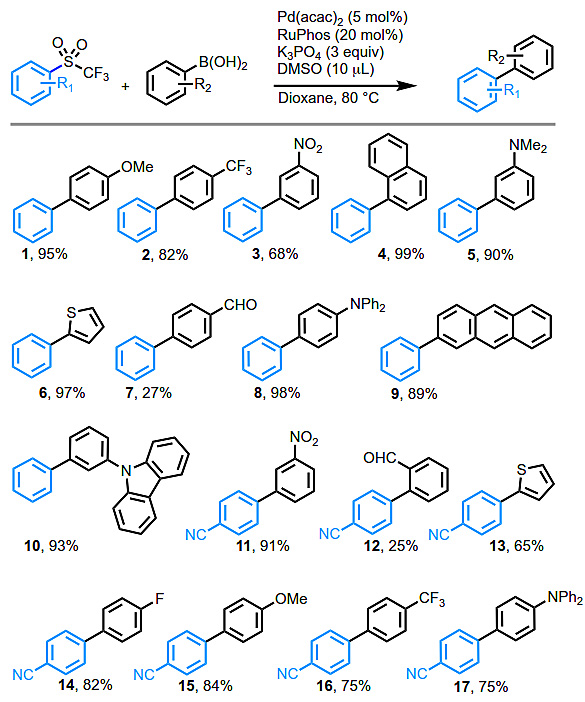
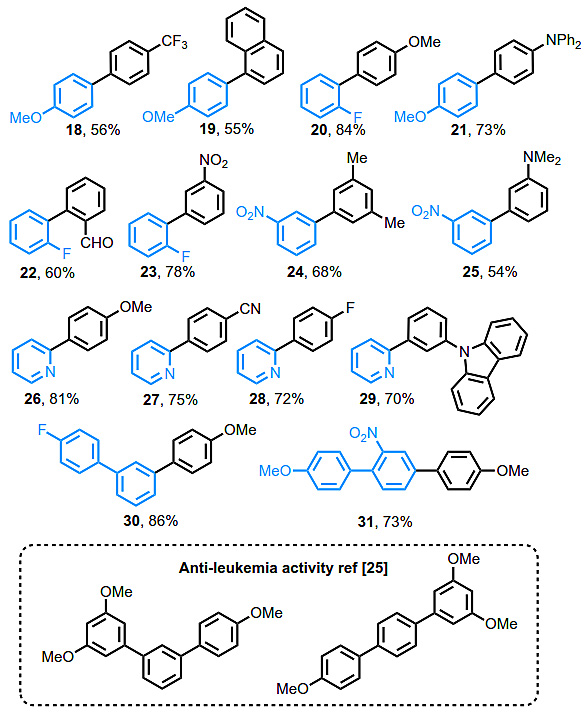
图3. 对照实验。图片来源:Angew. Chem. Int. Ed. 然后,作者利用优化的条件考察了各种芳基三氟甲基砜和芳基硼酸(图4)。在硼酸或砜上,给电子或吸电子基都能兼容。在含有硝基的底物(3,11,23-25,31)中会选择性在砜上发生偶联,这为利用最近发现的硝基SMC反应进行连续交叉偶联提供了可能性。大位阻硼酸也能以优异的产率(8-10,17,21和29)发生交叉偶联。噻吩硼酸也有良好的耐受性(6和13),而吡啶硼酸没有反应。2-氟芳基取代基对砜底物反应性没有影响(20,22,23)。2-吡啶砜(26-29)和间位、对位取代联苯基砜的交叉偶联产率良好,顺利得到30和31,后两种化合物是抗白血病化合物类似物。底物范围的主要局限性在于含醛基的硼酸,在某些情况下(7,12和22)交叉偶联产率较低。
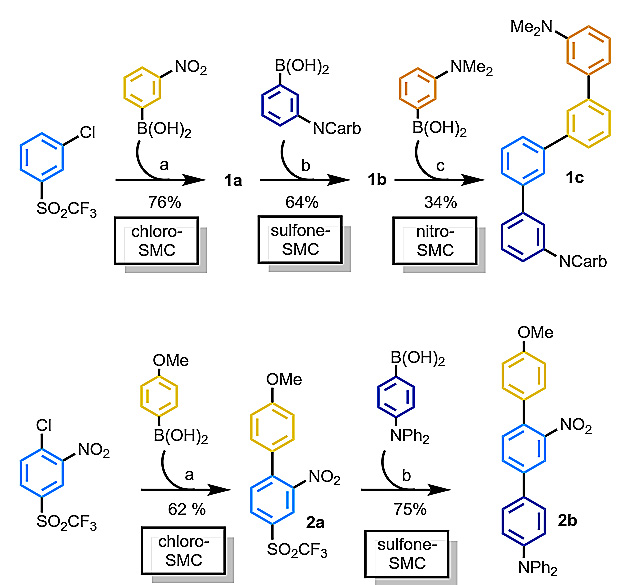
图4. 底物范围。图片来源:Angew. Chem. Int. Ed. 氯代芳烃(22 °C,以XPhos为配体)、芳基砜(80 °C,RuPhos为配体)和硝基芳烃(130 °C,以BrettPhos为配体)交叉偶联的反应条件相差甚远,基于此,作者开发了一种合成非对称三联和四联苯的连续SMC方法。2-氯苯基砜的氯与3-硝基苯硼酸发生SMC(chloro-SMC),生成联苯1a;接着是1a的砜基与4-N-咔唑基苯硼酸发生SMC(sulfone-SMC),得到三联苯1b;最后是1b硝基的SMC(nitro-SMC),产生四联苯1c。在同一芳环上还可以区分氯、砜和硝基等离去基,如1-氯-2-硝基-4(三氟甲基)砜基苯的氯选择性SMC得到联苯2a,其次才是砜选择性SMC得到2b。化合物30和31也能以类似的方式制备得到。
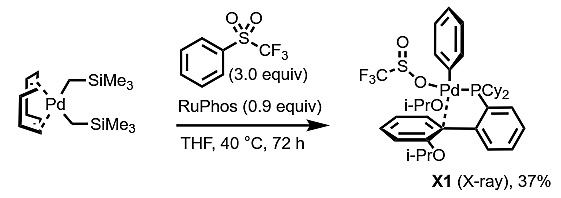
图5. 非对称三联和四联苯的合成。图片来源:Angew. Chem. Int. Ed. 为了了解反应机理,作者进行了Pd(0)前体(1,5-环辛二烯)双(三甲基硅烷基甲基)钯和PhSO2CF3之间的当量反应,制得并分离出了反应中间体X1(图6)。X1的X-射线晶体结构表明,在氧化加成后,钯与亚磺酸盐的氧结合,表明钯配合物在对C-S键氧化加成后会发生重排。这种结构与卤代芳烃和硝基芳烃的氧化加成结构相似,钯以平面正方形的几何形式存在。X1与4-甲氧基苯硼酸在25 °C标准条件下的当量反应,以接近定量的产率得到了联芳基化合物1,表明氧化加成是催化循环中的决速步骤。在非标准条件下,使用X1(5 mol%)将4-甲氧基苯硼酸和PhSO2CF3偶联,以62%的产率得到1,而过量Ruphos(20 mol%)的存在将产率提高到95%,这表明过量的Ruphos延迟催化剂分解的能力有利于反应产率。为了跟踪离去基团,作者用D2O萃取粗反应混合物,用19F NMR检测到了三氟甲磺酸酯的存在。
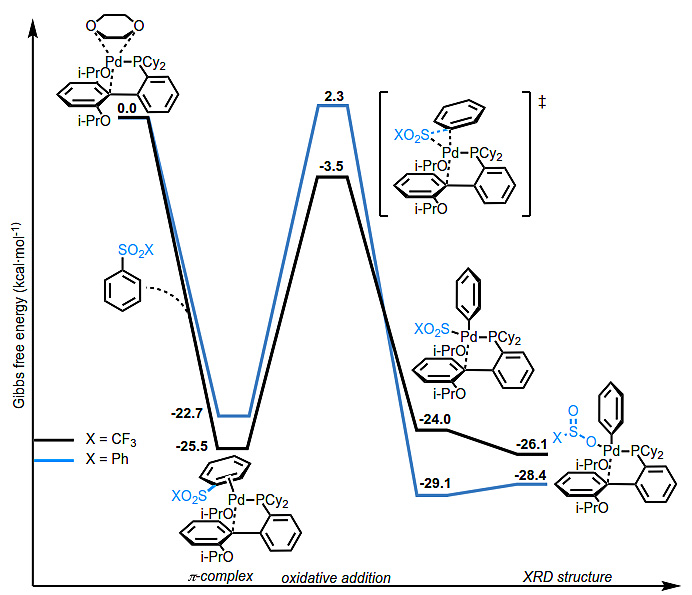
图6. 反应中间体X1的制备。图片来源:Angew. Chem. Int. Ed. 作者还用DFT计算进一步探讨了反应机理,补充了实验结果。由于上述实验支持氧化加成是循环决速步,在与具有挑战性亲电试剂的SMC反应中,第一步是配位溶剂分子(二氧六环)与底物的配体交换,形成π-配合物,对PhSO2CF3稍微有利(图7)。C-S键氧化加成的过渡态的Gibbs自由能,PhSO2Ph比PhSO2CF3的活化能高5.8 kcal/mol,与整个催化反应的实验趋势一致,与后续C-S键极性的增加相一致。S-键合的Pd中间体在能量上接近观察到的O-结合XRD结构X1。
图7. 计算的Gibbs自由能。图片来源:Angew. Chem. Int. Ed. 总结 Joseph Moran教授课题组报道了(杂)芳基砜的Suzuki-Miyaura交叉偶联反应,涉及钯对芳基砜C-S键的一种相对罕见的氧化加成。值得注意的是,三氟甲基砜反应活性介于硝基芳烃和卤代芳烃之间,通过连续交叉偶联可以仅用2到3步就顺利合成非对称的三联和四联苯基化合物。 原文(扫描或长按二维码,识别后直达原文页面,或点此查看原文):
Suzuki-Miyaura Coupling of (Hetero)Aryl Sulfones: Complementary Reactivity Enables Iterative Polyaryl Synthesis Paul Chatelain, Abhijit Sau, Christopher N. Rowley, Joseph Moran Angew. Chem. Int. Ed., 2019, DOI: 10.1002/anie.201908336 审校:龙须友 如果篇首注明了授权来源,任何转载需获得来源方的许可!如果篇首未特别注明出处,本文版权属于 X-MOL ( x-mol.com ), 未经许可,谢绝转载! 点击分享 收藏 取消收藏 评论: 1 |
【本文地址】
今日新闻 |
推荐新闻 |